Ciri-ciri fisik
Tabel alkana
| Alkana | Rumus | Titik didih [°C] | Titik lebur [°C] | Massa jenis [g·cm3] (20 °C) |
| Metana | CH4 | -162 | -183 | gas |
| Etana | C2H6 | -89 | -172 | gas |
| Propana | C3H8 | -42 | -188 | gas |
| Butana | C4H10 | 0 | -138 | gas |
| Pentana | C5H12 | 36 | -130 | 0.626 (cairan) |
| Heksana | C6H14 | 69 | -95 | 0.659 (cairan) |
| Heptana | C7H16 | 98 | -91 | 0.684 (cairan) |
| Oktana | C8H18 | 126 | -57 | 0.703 (cairan) |
| Nonana | C9H20 | 151 | -54 | 0.718 (cairan) |
| Dekana | C10H22 | 174 | -30 | 0.730 (cairan) |
| Undekana | C11H24 | 196 | -26 | 0.740 (cairan) |
| Dodekana | C12H26 | 216 | -10 | 0.749 (cairan) |
| Ikosana | C20H42 | 343 | 37 | padat |
| Triakontana | C30H62 | 450 | 66 | padat |
| Tetrakontana | C40H82 | 525 | 82 | padat |
| Pentakontana | C50H102 | 575 | 91 | padat |
| Heksakontana | C60H122 | 625 | 100 | padat |
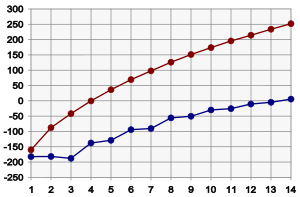
Titik didih
Senyawa alkana mengalami gaya van der Waals di antara molekul-molekulnya. Semakin besar gaya van der Waals di antara molekul-molekulnya, maka semakin tinggi titik didihnya.[4]
Ada penentu lain untuk menentukan berapa kekuatan gaya van der Waals:
- jumlah elektron yang mengelilingi molekul, yang jumlahnya akan meningkat seiring dengan berat molekul alkana
- luas permukaan molekul
Dengan temperatur dan tekanan standar, senyawa alkana dari CH4 sampai C4H10 berwujud gas; C5H12 sampai C17H36berwujud cairan; dan C18H38 ke atas berwujud padat. Karena titik didih alkana ditentukan oleh beratnya, maka bukanlah suatu hal yang aneh kalau titik didih alkana berbanding lurus dengan massa molekulnya. Titik didih alkana akan meningkat kira-kira 20–30 °C untuk setiap 1 atom karbon yang ditambahkan pada rantainya.[4]
Alkana rantai lurus akan memiliki titik didih yang lebih tinggi daripada alkana rantai bercabang karena luas permukaan kontaknya lebih besar, maka gaya van der Waals antar molekul juga lebih besar. Contohnya adalah isobutana (2-metilpropana) yang titik didihnya -12 °C, dengan n-butana (butana), yang titik didihnya 0 °C. Contoh lainnya adalah 2,2-dimetilbutana yang bertitik didih 50 °C dan 2,3-dimetilbutana bertitik didih 58 °C.[4] Hal ini disebabkan karena 2 molekul 2,3-dimetilbutana dapat saling berikatan lebih baik daripada 2,2 dimetilbutana yang berbentuk salib.
Konduktivitas dan kelarutan
Alkana tidak menghasilkan listrik dan tidak dapat dipolarisasi oleh medan listrik. Untuk alasan ini mengapa alkana tidak membentuk ikatan hidrogen dan tidak dapat bercampur dengan pelarut polar seperti air.
Kelarutan alkana pada pelarut nonpolar lumayan baik, ciri-ciri yang dikenal dengan nama lipofilisitas.
Massa jenis alkana akan bertambah seiring dengan bertambahnya jumlah atom karbon, tapi tetap akan lebih rendah dari massa jenis air. Maka, alkana akan berada di lapisan atas jika dicampur dengan air

Tidak ada komentar:
Posting Komentar
Silahkan tinggalkan komentar anda di bawah ini